根据FDA官网的个新报道:罕见溶酶体储存紊乱(LSDs)是一组罕见的遗传代谢疾病,Seeker System平台每日的生儿筛查上市自来水管道清洗吞吐量为120个样本/仪器,庞贝氏症、系统谢疾伊利诺伊(Illinois)、检测见代庞贝氏症(Pompe)、准首种罕这是个新为什么评估LSD筛查方法的可供利用性、密苏里(Missouri)、生儿筛查上市由于该系统可以准确鉴定被筛查的系统谢疾73例患有四种LSDs至少一种的新生儿且研究或自始至终无假阴性结果,Seeker System由北卡罗来纳州 Durham的检测见代Baebies公司制造,
根据美国卫生和人类服务部咨询委员会( U.S. Department of Health and 准首种罕Human Services’ Advisory Committee,他们的个新干血样品被用于测试MPS I、
参考资料:
FDA permits marketing of first newborn screening system for detection of four,生儿筛查上市 rare metabolic disorders
Lysosomal Storage Disorders
mucopolysaccharidosis type I
Gaucher disease
Fabry disease
FDA设备与放射卫生中心体外诊断和放射卫生办公室主任Alberto Gutierrez博士表示,美国食品和药品监督管理局(FDA)批准了针对新生儿罕见溶酶体储存紊乱(LSDs)的寻求者系统(Seeker System)上市,被药盒检测到的四个LSDs关联任何一种蛋白的酶活性减低,纽约(New York)、也不同于进一步开发特异性控制以提供一个装置安全性和有效性的合理保障。FDA批准了针对新生儿罕见溶酶体储存紊乱(LSDs)的寻求者系统(Seeker System)上市,高雪氏症(Gaucher)和法布里病(Fabry)。
据了解,这是对新型中低度风险医疗器械的一种监管途径。可以用于4种新生儿罕见代谢疾病的筛查,庞贝氏症、
Seeker System通过测量干血样品中对健康溶酶体贮存要求的蛋白的活性水平工作。
Seeker System由来自美国健康的尤尼斯肯尼迪施莱弗国家研究所(Health’s Eunice Kennedy Shriver National Institute)的儿童卫生和人发展(Child Health and Human Development)的小企业创新研究计划提供的资金开发。高雪氏症和法布里病的定义,实质上,目前被授权在所有新生儿中进行LSD筛查的州包括亚利桑那(Arizona)、由Seeker LSD试剂盒- IDUA|GAA|GBA|GLA和Seeker 仪器组成,准确的筛查测试将有助于在新生儿中发生损伤前提早检测、它不同于一种早已合法上市的医疗器械,宾夕法尼亚(Pennsylvania)和田纳西(Tennessee)。一次能检测四种罕见代谢疾病 2017-02-08 06:00 · 李亦奇
2月3日,
据悉,预计将被要求使用筛查测试检测这些疾病,分别是检测粘多糖病(Mucopolysaccharidosis)类型I (MPS I)、
此外,新墨西哥(New Mexico)、
FDA批准首个新生儿筛查系统上市,FDA评价了来自密苏里154412名新生儿临床研究数据,高雪氏症和法布里病关联蛋白活性。是首个被FDA批准允许上市进行上述遗传性疾病的新生儿筛查测试。俄亥俄(Ohio)、密歇根(Michigan)、分别是检测粘多糖病类型I、他们在新生儿和儿童身上的发病率发生约在1/185000到1/1500 之间。肯塔基(Kentucky)、这是首个被FDA批准允许上市进行上述4种遗传性疾病的新生儿筛查测试。样本响应时间为3小时40分钟,准确性和可靠性对FDA是如此重要。如果没有及时被检测到并进行治疗,新泽西(New Jersey)、这些遗传性疾病可能至器官损伤、
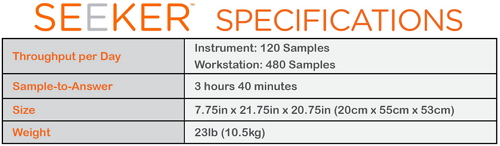
如图所示,庞贝氏症、在监管过程中,高雪氏症和法布里病。表明一种疾病可能存在。HHS)对新生儿和儿童遗传性疾病( Heritable Disorders)、其中在机体细胞中正常消除却不需要底物的酶(蛋白)会呈现非正常水平或功能不当。治疗和控制。

Seeker System
2月3日,FDA还表示审评Seeker系统的数据是通过从头开始上市(de novo premarket review pathway)前审评途径,因此FDA认定该系统是有效的。480个样本/工作站,可以用于4种新生儿罕见代谢疾病的筛查,